IP、Co-IP、Pull-down 快速区分
一、概念
(一)免疫沉淀(Immunoprecipitation,IP)
该技术利用抗原与抗体的特异性反应,从不均一的细胞或组织提取物中富集特定蛋白质。在免疫沉淀过程中,利用抗体结合目标蛋白,通过添加Protein A/G磁珠等亲和层析介质来沉淀复合物,利用磁珠的磁性用磁架收集抗原-抗体复合物,通过洗涤去除未结合的物质,获得富集的蛋白。
(二)免疫共沉淀(Co-immunoprecipitation,Co-IP)
该技术的操作过程与前者并无区别。不同之处在于针对富集的蛋白样品,一个样本检测两个或多个蛋白质,从而探究诱饵蛋白的互作蛋白质。因样本来源于生物体的细胞或组织,免疫共沉淀的结果更还原体内蛋白质之间的相互作用。该技术不能证明蛋白质之间的互相作用是直接的还是间接的。比如A诱饵的沉淀样本中检测B蛋白,并不意味着A-B直接结合,存在A-C-F-D-B或A-D-B-F等间接结合的可能性。
(三)Pull-down
该技术是通过体外表达带标签的诱饵蛋白(如GST/His标签),利用标签以及亲和柱的特异性结合,检测与诱饵蛋白互作的其他蛋白质。根据实验设计的不同,可以分为两种类型:
1粗提物Pull-down:重组标签蛋白与细胞/组织裂解液孵育,用于筛选与诱饵蛋白结合的候选互作蛋白。此方案不能区分直接或间接作用。
2纯化蛋白Pull-down:两种蛋白均为重组纯化(如GST-A+His-B),在体外无其他蛋白存在的条件下进行结合实验。若检测到相互作用,则代表两者存在直接结合。
Pull-down实验与Co-IP实验其实是相互补充的两种实验方法,通过二者结合,我们才能更准确地了解两个蛋白之间的真实互作情况。
二、实验流程
(一)IP和co-IP的Protocol
1. 样品制备:
① 配制细胞裂解液:称取150 mM NaCl,50 mM Tris-HCl (PH = 8.0),10 mM MgCl2,0.5%(v/v)Triton X-100,10%(v/v)甘油,过滤后4℃保存。使用时1:100比例添加适量的
蛋白酶抑制剂(PI)和PMSF。
② 以Jurkat细胞为例,收集细胞并计数,取4 × 107个细胞,1000 rpm室温离心5 min,然后再用预冷的PBS洗涤三遍。
③ 加入2 mL的细胞裂解液(使用前加入PI和PMSF),分装为两个EP管中,每管各1 mL,封口膜封口并放于4℃摇床裂解30 min。裂解完成后,4℃条件下12000 g离心15 min。将上清转移至新的EP管中,最后取80 μL加入适量的5 × loading buffer,最后98℃煮样10 min,作为Input阳性对照。
2. 平衡树脂:
取240 μL的50% protein G sepharose 4B树脂,加入1 mL细胞裂解液洗涤,然后4℃条件下1700 rpm离心4 min,洗涤三遍。最后一次弃去上清并加入120 μL细胞裂解液重悬树脂。
3. 预吸附:
每1 mL的细胞裂解液(步骤2所得的)加入60 μL的50%平衡树脂,放置于4℃水平摇床上摇晃1 h。预吸附结束后,4℃条件下1700 rpm离心4 min,收集上清到另一洁净EP管中。
4. 抗体结合:
① 将细胞裂解液平均分到2个EP管中,每管加入不同的抗体,对照组加入对照的同种非特异性抗体4 ug,实验组加入特异性抗体4 ug,并放置于4℃层析柜中摇动结合过夜。
② 结合过夜后,分别加入60 μL的50%平衡树脂,4℃层析柜摇动3-4 h。
5. 洗涤树脂:
4℃条件下1700 rpm离心4 min,小心去掉上清,使用细胞裂解液重复洗涤三次。洗涤完成后加入等体积2 × loading buffer,并放于98℃煮样5 min,瞬时离心后放-20℃保存。
6. 检测:
Western blot检测,上样之前涡旋震荡后瞬时离心。每组各取5 μL样品用于检测IP下来的蛋白,另外每组各取20 μL样品用于分析免疫共沉淀的蛋白。
7. 结果解析
通常检测如图1所示,该文章通过co-IP验证CDKL3和Akt是否存在相互作用,以Akt抗体富集该Akt蛋白,在③泳道检测出CDKL3与Akt的存在,表明该样本中两个蛋白存在相互作用。
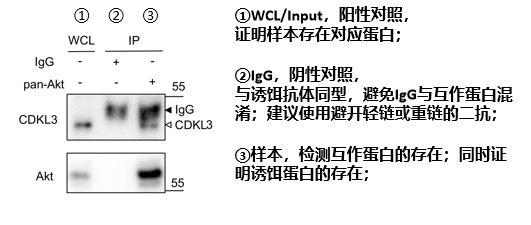
图1 Co-IP免疫印迹结果图[1]
(二)Pull down的Protocol
1. 质粒构建:
① 利用已知含有特定蛋白的样本cDNA,PCR扩增目的蛋白的DNA片段;
② 通过基因工程技术(酶切、酶连/重组),将该序列重组至合适的表达载体上(以GST标签为例使用pGEX-4T-1质粒);
③ 将重组质粒转化至Stbl3感受态,过夜培养,挑取单克隆进行菌落PCR鉴定、测序分析;
2. 转化:将验证过的pGEX-4T-1-A重组质粒转化至大肠杆菌Rosetta菌株;
3. 诱导表达:
① 挑取平板上的单个克隆,转移至含Amp抗生素的5 mL LB液体培养基中,37℃摇菌过夜,制备种子液(12-16 h);
② 将菌液转移至含Amp抗生素的500 mL 的LB锥形瓶中,37℃,250 rpm培养至OD600为0.4-0.6;
③ 加入终浓度为0.1 mM的IPTG,在18℃条件下培养12 h。
4. 破碎菌体:
① 4℃,3800 g离心10 min收集细菌,弃去上清。菌体可以直接纯化或放置于-20℃保存。取出菌体,立刻放置于冰盒上,每50 mL培养基得到的菌体加入6 mL预冷的含1 mM PMSF的裂解液(50 mM Tris-HCl,1% Triton X-100,150 mM NaCl,pH=8.0),吹打混匀;
② 使用漩涡振荡仪振荡悬浮菌液,然后将菌液转移至10 mL的离心管中,每管约6 mL,冰水混合物上低温超声破碎,超声破碎的条件为破5 s,停10 s,总共破碎20次,直至裂解液充分澄清为止;
注:细菌破碎时,应将离心管置于冰水中,避免蛋白质因产热变性。同时,细菌破碎的条件需自行优化。
③ 4℃,10000 g离心10 min,上清转移至另一干净的10 mL离心管中,重复离心一遍,然后上清再转移到另一干净的10 mL离心管中,-80℃保存备用;
5. 纯化:
① 取500 μL GST-Beads(Immobilized Glutathione)到EP管中,用1 mL细胞裂解液润洗三次,将冻融的融合蛋白GST-A与树脂混匀,4℃层析柜旋转结合30 min。500 g低温离心5 min,弃去上清,并加入1 mL的细胞裂解液洗涤三次。
② 同时制备细胞裂解液,裂解液(50 mM Tris-HCl,1% Triton X-100,150 mM NaCl,pH=8.0),按照1:100的比例添加蛋白酶抑制剂PI。
注:大量纯化时,利用低压层析系统,细菌裂解液上清液转移至GST binding buffer预平衡的GST亲和层析柱;用binding buffer冲洗层析柱,至流出液的OD280值到达基线;用GST Elution buffer洗脱目的蛋白,收集流出液;收集的蛋白溶液加入透析袋中,使用Tris-HCl透析过夜;进行SDS-PAGE电泳,对凝胶进行考马斯亮蓝染色,染色过夜后脱色处理,观察目的蛋白是否大量表达;(详细参考使用的试剂盒说明书资料)
6. 检测:
① 将结合有GST融合蛋白的谷胱甘肽树脂悬浮在缓冲液中,加入含有其他纯化蛋白(FLAG-B)的溶液,同时采用结合有GST空蛋白的谷胱甘肽树脂平行操作作为对照组;
② 4℃旋转结合3h,1800 rpm离心4 min,弃去上清;再加入缓冲液对树脂进行洗涤,重复2-3次;
③ 加入适量 loading buffer,98℃煮样5 min;SDS-PAGE以及WB检测B蛋白。
7. 结果解析:
以图2为例,该文章通过GST-ZBED3和GST-PRMT5分别下拉了FLAG-PRMT5与FLAG-ZBED3,表明这两个蛋白存在直接相互作用。
若检测样本类型为细胞裂解液,则结果以图3为例。该结果表明ORP4L与ITPR1(2615-2695)存在相互作用,是否是直接的未知。
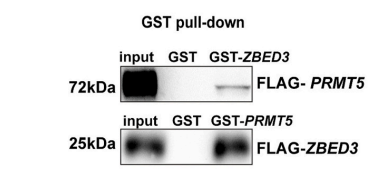
图2 GST pull-down免疫印迹结果图[2]
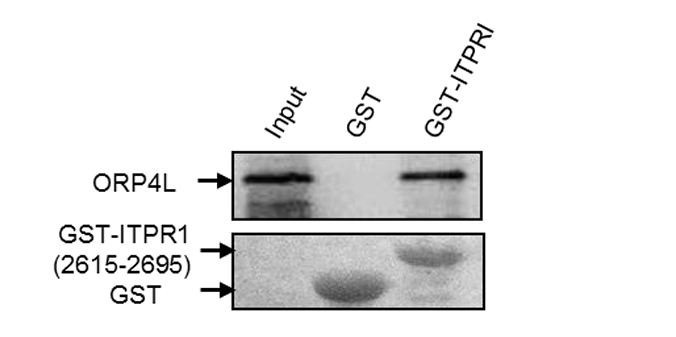
图3 GST pull-down免疫印迹结果图[3]
三、常见问题与建议
|
常见现象 |
可能的原因 |
解决方案 |
|
无沉淀、 |
抗体亲和力低 |
更换抗体,选用IP专用抗体 |
|
目的蛋白表达量低 |
增加裂解液用量或WB上样量 |
|
|
抗原抗体无法结合 |
使用更温和的裂解液 |
|
|
抗原表位被遮蔽 |
优化裂解条件(避免过度超声) |
|
|
高背景 |
抗体特异性差 |
使用特异性更好的抗体 |
|
抗体浓度过高 |
降低抗体用量 |
|
|
封闭不充分 |
增加封闭时间(建议选择BSA封闭) |
|
|
洗涤不充分 |
增加洗涤次数 |
|
|
预吸附不彻底 |
延长预吸附处理时间,吸附去除样品中的非特异杂质 |
|
|
轻重链干扰 |
二抗识别抗体的IgG |
建议选用IP专用二抗(避开轻链或重链) |
|
获得的蛋白量低 |
蛋白质被降解 |
加入蛋白酶抑制剂,确保实验全程低温进行 |
|
磁珠不够用 |
提高捕获免疫复合物所使用的磁珠量 |
|
|
样品中目标蛋白含量低 |
提高细胞数 |
|
|
Input组无条带 |
Input中目的蛋白含量较低,IP富集提高含量而被检测到 |
增加Input上样量 |
|
磷酸化或修饰蛋白的表达水平低 |
某些靶标可能在特定条件下诱导表达;许多翻译后修饰蛋白本底表达水平较低 |
对于磷酸化蛋白的检测,裂解液中同时添加混合型蛋白酶抑制剂和磷酸酶抑制剂 |
四、参考文献
[1] He A, Ma L, Huang Y, et al. CDKL3 promotes osteosarcoma progression by activating Akt/PKB. Life Sci Alliance. 2020;3(5):e202000648. Published 2020 Mar 31.
[2] Luo YY, Ruan CS, Zhao FZ, et al. ZBED3 exacerbates hyperglycemia by promoting hepatic gluconeogenesis through CREB signaling. Metabolism. 2025;162:156049.
[3] 李超文. OSW-1 抑制 ORP4L 的功能导致 T-ALL 细胞的死亡[D]. 暨南大学, 2018.